摘要
放射治疗通过诱导免疫原性细胞死亡(ICD)激发抗肿瘤免疫,但单纯的局部同位素治疗常面临核素易流失、靶区剂量不足的物理局限。更为棘手的是其生物学悖论:电离辐射会诱发肿瘤微环境(TME)生成大量中性粒细胞胞外诱捕网(NETs)。这些致密的NETs不仅赋予肿瘤辐射抗性,也构成物理与生化屏障,阻断效应T细胞浸润,进而削弱抗肿瘤免疫甚至促发转移。基于此,当前亟待解决的核心科学问题是:如何构建一种高效的局部递送系统,在实现放射性核素长效精准锚定的同时,时空同步地清除由辐射诱发的NETs免疫抑制屏障?针对这一关键问题,研究团队开发了一种光固化原位水凝胶递药系统,共载同位素碘-131与脱氧核糖核酸酶 I(DNase I)。瘤内注射并交联固化后,该载体既实现了131I的长效近距离放疗,又通过缓释DNase I精准降解NETs结构。本文将系统解析该策略如何逆转放疗诱导的免疫逃逸,成功打通“局部放疗——微环境重塑——全身免疫激活”的治疗闭环。

一、研究背景与核心科学问题:
1.研究背景:放射性同位素治疗面临两大瓶颈:一是核素瘤内滞留期短;二是放疗诱导的微环境免疫抑制。后者主要源于电离辐射诱发的中性粒细胞胞外诱捕网(NETs)异常聚集;该致密理化屏障不仅直接介导肿瘤放射抵抗,而且严重阻滞效应T细胞浸润,最终削弱系统性抗肿瘤免疫并促发远端转移。
核心科学问题:在克服放射性同位素瘤内滞留时间短这一物理缺陷的同时,应如何有效消除电离辐射诱发NETs所导致的肿瘤放射抗性与免疫逃逸,进而实现放射-免疫联合治疗疗效的最大化?
核心假设:基于原位固化水凝胶的双效递送系统(131I/DNase I),通过“长效靶向放疗”与“NETs精准降解”的时空协同,可根本性阻断辐射诱发的微环境免疫抑制负反馈,进而将局部免疫原性细胞死亡(ICD)最大化转化为系统性抗肿瘤免疫应答。
二、研究设计总览:从“局部靶向滞留”到“系统免疫转化”的完整证据链
本研究遵循“载体构建 →药代评估
→微环境重塑 →免疫重编程 →远隔效应验证”的递进逻辑,构建了严密的因果论证闭环:
1. 材料学构建与双效释药机制:设计并表征了基于甲基丙烯酰化羧甲基壳聚糖(CMCSMA)的光固化水凝胶。通过Iodogen法共价标记同位素131I并物理包埋DNase I,奠定“同位素原位锚定”与“生物酶长效缓释”的物理载体基础。
2. 局部药代动力学与滞留验证:借助SPECT活体成像与组织生物分布定量,证实原位成胶可将131I的肿瘤局部有效滞留期显著延长至7天以上。此举排除了游离核素系统性泄露的毒性干扰,确立了长效近距离放疗的物理学前提。
3. 微环境生化清障的靶向确认:基于组织免疫荧光技术,确证电离辐射在诱发免疫原性细胞死亡(ICD)的同时激增NETs。进而证实共递送的DNase I靶向切断了Cit-H3/MPO网络,完成从“单纯药物释放”到“实质性消除微环境理化屏障”的机制确证。
4. 局部免疫微环境重编程解析:将NETs屏障的消除转化为免疫表型逆转的实质性证据。流式细胞术解析证实,靶向降解NETs可显著促使效应CD8+ T细胞深层浸润,驱动巨噬细胞向抗肿瘤M1型极化,并下调免疫抑制性Treg细胞比例,完成局部免疫重编程的机制衔接。
5. 系统疗效与远隔效应(Abscopal Effect)验证:以双侧皮下瘤模型为最终疗效终点,检验局部干预的全身转化能力。证实原发灶的“放疗+酶解”协同策略不仅有效控制受照靶区,更成功激发系统性适应性免疫反应,显著消退远端未受照转移灶并延长总体生存期,形成“局部干预→机制阻断 →全身获益”的完整验证闭环。
3.1 递送系统构建: 131I-CMCSMA/DNase I 复合水凝胶的理化表征与释药动力学
1.材料与平台:以甲基丙烯酰化羧甲基壳聚糖(CMCSMA)为聚合物基质,利用Iodogen法共价标记同位素131I,并物理包埋DNase I。该体系在405 nm紫外光下10秒内即可完成光引发交联,形成稳定的三维水凝胶网络。
2.结构与释药属性:SEM表征显示凝胶呈高孔隙率的三维微观结构,有利于生物酶的负载与释放。体外释药动力学证实,该体系能长效锚定131I 14天保留率达58.8%),同时实现大分子蛋白(模拟DNase I)的pH响应性持续缓释,并在活体皮下呈现31天的可控降解周期。
该体系的核心目的在于满足“放射线空间精准锚定”与“生物酶时间可控缓释”的物理前提,从而为构建局部放射-免疫微环境提供剂量稳定的储库。然而,该平台在实现物理递送的同时,是否具备充分的生物安全性并保留DNase I的降解活性,仍需在体外进行前置验证。
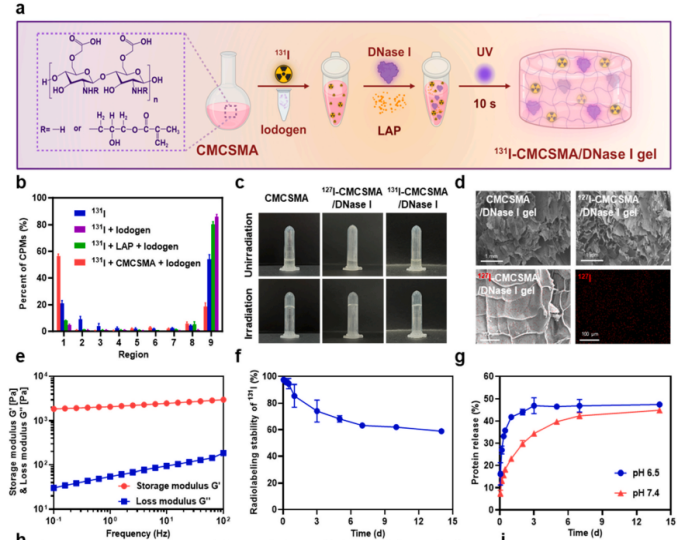
图1: 131I-CMCSMA/DNase I 凝胶的制备、理化表征与流变学/释放动力学分析
3.2 关键前置验证:水凝胶平台的生物相容性与靶向降解NETs活性确认
在生物安全性方面,CMCSMA聚合物及不同浓度的凝胶浸提液在24小时内对CT26结直肠癌细胞均维持高存活率(>80%),排除了材料自身毒性对后续免疫微环境表型评估的非特异性干扰。 在生化功能活性方面,利用PMA刺激dHL-60细胞形成典型NETs,并且凝胶浸提液能与游离DNase I同等有效地显著降低NETs特异性标志物(Cit-H3与MPO)的荧光信号,证实载体释放的DNase I充分保留了切断胞外DNA网络的生物学活性。
体外结果确立了材料的安全性和生化活性基础。下一步的关键在于回答:在活体复杂生理环境中,该系统能否真正实现同位素的局部滞留,并初步转化为抑制原发肿瘤的病理学表型?
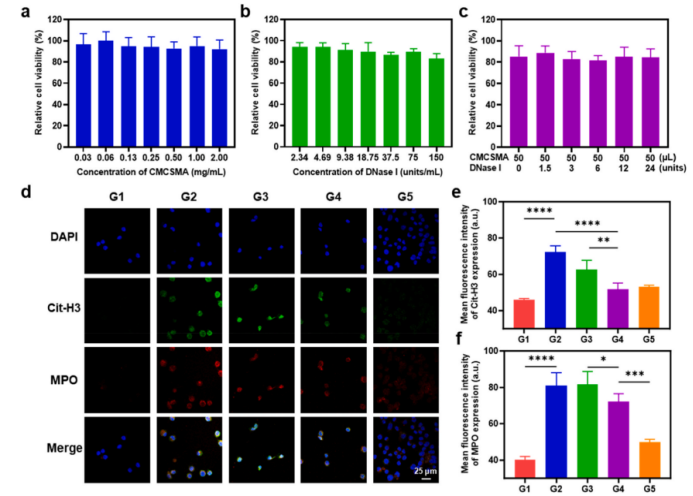
图2:体外CMCSMA/DNase I凝胶浸提液的细胞毒性评估与介导的NETs降解验证
3.3 活体药代与功能初探:长效滞留确立物理基础,协同干预抑制原发肿瘤
1.活体滞留确认:SPECT成像及组织生物分布定量(%ID/g)证实,瘤内注射的游离 131I迅速流失至甲状腺,而水凝胶组成功将核素在肿瘤局部的有效滞留期延长至7天以上。这一体内药代动力学证据确立了“长效近距离放疗”的物理可控性。
2.原发瘤抑制表型:在CT26单侧皮下瘤模型中,131I单核素凝胶已显现出初步的肿瘤抑制作用;而加入酶的双效凝胶(131I-gel/DNase I)展现出更显著的组织破坏学证据(H&E染色)及原发瘤生长抑制趋势。
活体证据证实了局部滞留与初步抑瘤效应,双效凝胶对原发瘤的抑制优势相比单核素组仅呈中度提升。为解释这一表型差异并挖掘其分子基础,亟需从“宏观疗效”向“微环境机制”推进:放疗究竟如何重塑了肿瘤微环境?DNase I的靶向清障又引发了哪些生化级联反应?
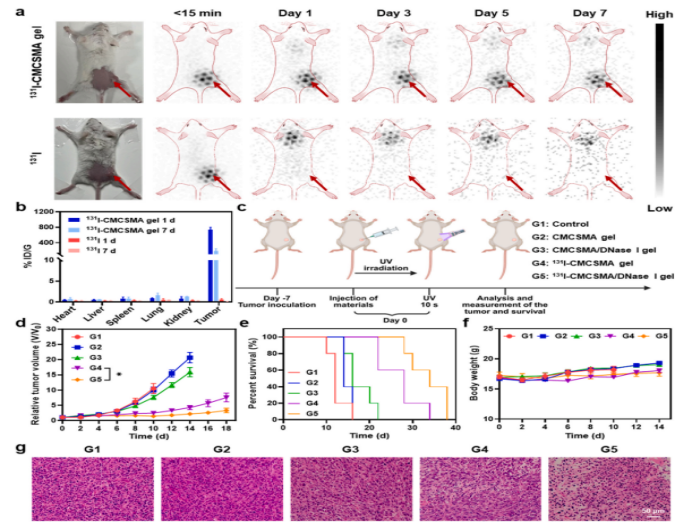
图3: 131I-CMCSMA/DNase I 凝胶的活体组织分布与原发瘤生长抑制曲线
3.4 微环境生化重塑:证实放疗诱导NETs免疫屏障及DNase I的靶向清障机制
为将研究从“疗效描述”推进至“分子机制确证”,研究提取治疗后肿瘤组织进行原位免疫荧光深度解析。
1.机制现象确认:组织切片揭示,单纯131I放疗在诱导基质发生微环境改变时,导致Cit-H3/MPO共定位信号大面积激增,直接提供了电离辐射诱发致密NETs屏障的实质性病理证据。
2.靶向清障与ICD放大:在双效凝胶干预下,NETs网状结构被显著瓦解,并且,肿瘤组织内的DNA损伤与免疫原性细胞死亡(ICD)标志物(CRT上调,HMGB1核外排)获得了显著的二次放大效应。
上述生化层面的证据证实,DNase I作为微环境调节剂,其核心功能在于瓦解NETs介导的放射抗性并放大ICD效应。既然致密的物理屏障已被降解,这一局部生化改变是否能实质性重编程肿瘤内的免疫细胞浸润网络,并最终决定系统性治疗终点?
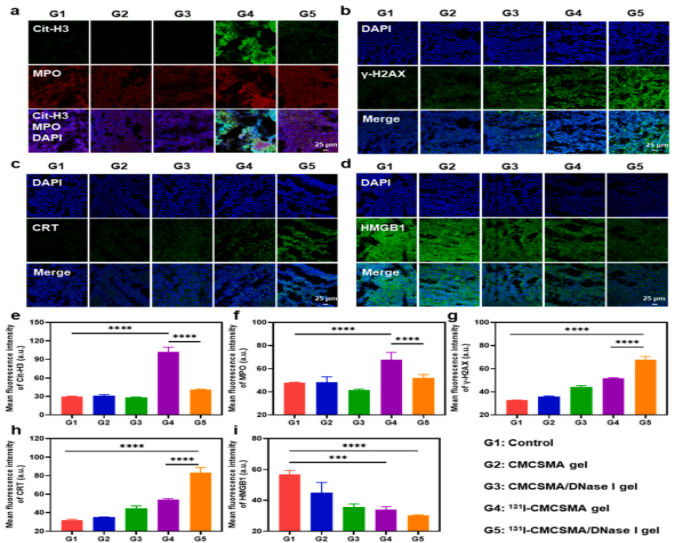
图4:活体肿瘤组织内NETs的靶向降解确认与ICD效应的荧光半定量分析
3.5 机制闭环与必要性检验:免疫重编程驱动远隔效应(Abscopal Effect)
前期已证实微环境的生化重塑,本阶段最终需验证其是否转化为真实的适应性免疫应答及系统性生存获益。
1.微环境免疫表型逆转:流式细胞术解析表明,清除NETs后,双效凝胶组肿瘤内的效应CD8+ T细胞浸润比例显著升至12.1%,而免疫抑制性Tregs比例显著下调;同时,巨噬细胞从促瘤的M2型发生向抗瘤M1型的强效极化。外周血中TNF-α的显著上调进一步证实了系统性抗肿瘤免疫的全面激活。
2.必要性与系统疗效检验:利用双侧瘤模型(仅局部干预原发灶,监测远端转移灶)进行终点验证。结果显示,相比于单核素放疗,双效凝胶组在远端未受照肿瘤中展现出压倒性的生长抑制能力,并大幅度延长小鼠终点生存期。
3.完整机制链条:局部长效放疗 诱发ICD的同时激增NETs理化屏障
DNase I原位缓释
靶向降解NETs网络
解除免疫细胞浸润阻滞
效应T细胞与M1巨噬细胞重塑微环境
激活系统性免疫记忆并引发远隔效应。这一证据链最终确证了:时空同步降解NETs,是最大化局部放疗系统性免疫收益的绝对必要条件。
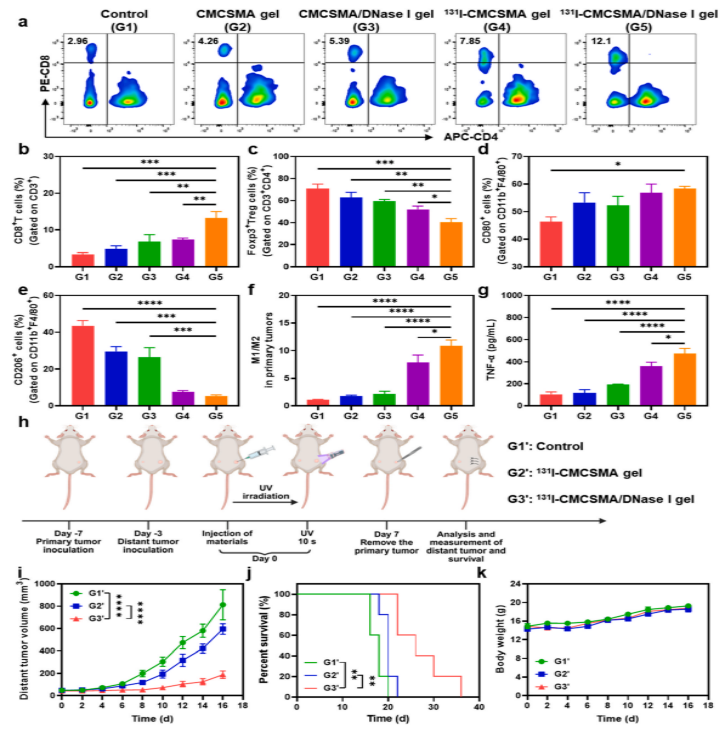
图5:肿瘤浸润免疫细胞群的流式细胞学表型分析与远端转移肿瘤的系统性疗效评估
四、创新点剖析
1.将放疗诱发的微环境副产物(NETs)从“被动承受的抗性背景”,提升为决定放免联合疗效的“核心上游可干预靶点”,重塑了放射免疫治疗的底层干预逻辑。
2.创新性整合高分子材料学与同位素药代动力学,利用原位光固化水凝胶同步克服了“游离核素易流失”与“游离生物酶半衰期短”两大递送瓶颈。
3.递送机制的精细化区分:聚合物骨架通过Iodogen法共价标记 131I(防泄露),同时物理包埋 DNase I(促缓释),在单一物理储库中完美实现了“近距离物理放疗”与“长效微环境生化清障”的时空同步。
总体归纳:研究构建了131I-CMCSMA/DNase I 双效原位水凝胶平台,在成功规避核素系统性毒性及流失的前提下,系统确证了DNase I介导的NETs靶向降解效能。结合组织微环境表征、免疫细胞流式组学及远端肿瘤干预终点,建立了“局部长效放疗—靶向降解NETs—CD8+ T细胞/M1巨噬细胞依赖的系统性远隔效应”的完整证据链闭环。
五、局限性及展望
1.物理触发深度受限:水凝胶的原位交联高度依赖405 nm紫外光(UV)照射,其组织穿透深度极浅,严重限制了该递送系统在肝、肺、胰腺等深部实体瘤中的无创或微创临床应用。
2.模型生理相关性差距:当前验证主要依赖小鼠皮下同基因移植瘤(CT26)模型,该模型缺乏人类消化道原位肿瘤的高度异质性、复杂的天然组织间质(ECM)网络以及长期的微环境演化过程,可能高估了远隔效应的实际临床响应率。
3.临床转化与工程学壁垒:作为同时糅合了放射性同位素、聚合物基质与敏感生物酶(大分子蛋白)的复合制剂,其大规模标准化GMP生产面临严峻挑战。尤其是终端灭菌工艺(常规的高温高压或高剂量辐照极易导致DNase I变性失活或凝胶网络降解),构成了实质性的药规转化障碍。
下一步亟待从底层材料学突破交联触发机制,开发非UV依赖的响应性平台(如体温相变、超声触发或深部微环境pH/酶响应型水凝胶),以满足原位深部肿瘤的靶向递送需求。同时,将药效学评价拓展至原位肿瘤模型或患者来源异种移植(PDX/PDO)模型,以在更接近临床真实基质的环境中验证其普适性。结合先进制剂与灭菌工艺(如无菌隔离器组装或差异化冷链加工),探索生物大分子与放射性核素的兼容性生产策略,有望真正补齐“概念验证—工艺放大—临床应用”的转化闭环,为克服难治性实体瘤的放射抗性提供具有高临床可及性的精准干预方案。